Серная кислота (Н2SО4) широко применяется в промышленности. Основное ее применение — в производстве суперфосфатов и сульфата аммония для удобрений. Серная кислота также используется в автомобильных аккумуляторах и в производстве некоторых синтетических волокон (например, вискозы), красителей, пластмасс, лекарств, взрывчатых веществ и моющих средств. Серная кислота используется в производстве диоксида титана — красителя, придающего краскам своеобразный цвет. 
Серная кислота — это разновидность минеральной кислоты. Минеральные кислоты состоят из элементов (в данном случае серы), встречающихся в виде минералов в земной коре. Концентрированная серная кислота очень активная и едкая. Растворяясь в воде, она выделяет много тепла, поэтому надо всегда добавлять ее в воду, а не наоборот. Так кислота быстрее растворяется, и тепло поглощается водой. Концентрированная серная кислота является сильным окислителем (во время процесса окисления она отдает кислород другим веществам). Она также является дегидратантом (удаляет воду, химически связанную с другими веществами). Если сахар нагреть с серной кислотой, кислота вытянет воду из сахара. В результате получится пенистая масса из черного углерода и воды. 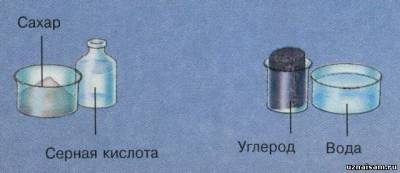
Убедись сам
Ты можешь провести собственный тест, чтобы определить кислотность или щелочность какого-либо вещества.
Для этого вначале сделай индикатор из красной капусты. Нарежь три больших капустных листа и свари в 0,5 л воды в течение десяти минут. Отвар остуди и разлей по небольшому количеству в три банки. Добавь половину чайной ложки соды в одну банку, немного уксуса в другую и дождевой воды в третью.
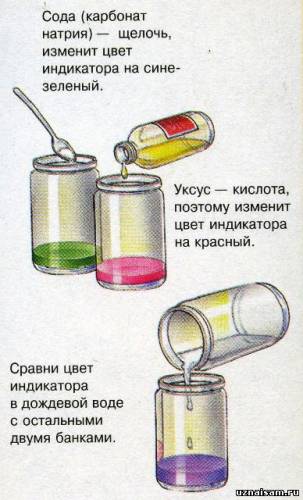
Если дождевая вода имеет кислотный уровень рН, индикатор порозовеет.
|